Ministerio de Salud de la Provincia de Buenos Aires,
Ministerio de Ciencia, Tecnología e Innovación
Instituto Leloir‐ CONICET‐INBIRS‐UNLP
Argentina se encuentra, desde enero de 2021, en el inicio de un proceso de vacunación masiva. Uno de los mayores problemas que enfrentamos a nivel mundial en la pandemia causada por SARS-COV2 es la escasez de vacunas y la disparidad en su distribución. La primera vacuna recibida y la más utilizada hasta la fecha en nuestro país es Sputnik V. Sobre esta vacuna se han reportado informes sobre la eficacia y seguridad en estudios clínicos de Fase 3 (1). Sin embargo, es importante evaluar la respuesta inmune a ésta y otras vacunas en nuestra población. Asimismo, no existe información hasta el momento sobre la respuesta a la vacunación con Sputnik V de individuos previamente infectados con SARS-CoV-2. Al respecto, es necesario generar información local sobre la respuesta inmune a la vacunación y sobre el beneficio de aplicar una o dos dosis en los casos donde haya habido exposición previa al virus. Complementariamente, estas evidencias locales podrían aportar información para mejorar las campañas de donación de plasma dirigidas a alguna subpoblación de interés.
El esquema de vacunación de Sputnik V consta de un régimen de dos dosis con un intervalo de al menos 21 días entre la primera y la segunda dosis. En el presente estudio se realizó un análisis longitudinal de 142 individuos vacunados, hasta el momento se procesaron 609 muestras y se realizaron más de 3000 determinaciones. En el protocolo empleado, se tomaron muestras de suero previo a la vacunación (nivel basal), a los 21 días de haberse aplicado la primera dosis y a los 21 días de haberse aplicado la segunda dosis. La cohorte empleada en esta etapa está compuesta por personal de salud del subsector público de la Provincia de Buenos Aires de 18 a 59 años, muestras de otras cohortes se están recibiendo para un próximo análisis. El estudio continuará tomando muestras a los 3 y 6 meses luego de aplicada la primera dosis.
Para cada muestra de suero recibido se evaluó el título de anticuerpos de tipo IgG anti-S y anti RBD empleando el test de ELISA COVIDAR (2) y se determinó la funcionalidad de dichos anticuerpos mediante ensayos de neutralización con el sistema de virus pseudotipado VSV GFP, expresando la proteína Spike en su superficie. Asimismo se realizaron estudios empleando ensayos de neutralización con el virus SARS-CoV-2 cepa salvaje.
Los resultados obtenidos indican que a los 21 días de la primera dosis de la vacuna Sputnik V, el 89 % de los individuos analizados desarrolló anticuerpos IgG anti-Spike detectables, mientras que a los 21 días de la segunda dosis el 100% de los vacunados desarrolló estos anticuerpos.
La medición de los niveles basales de anticuerpos (previo a la vacunación) permitió dividir a los voluntarios en dos grupos. El grupo 1 (120 individuos) con anticuerpos de tipo IgG no reactivo a tiempo inicial (muestra basal), sin evidencia de exposición previa a SARS-CoV-2 y el grupo 2 (22 individuos) con anticuerpos IgG anti-Spike detectables, indicando previa infección. En la Figura 1 se puede observar la comparación del título de IgG en el nivel basal de ambos grupos.
Primera dosis: La respuesta humoral observada en individuos del grupo 2 después de la primera dosis fue robusta en todos los casos, alcanzando una mediana de títulos muy alta de 12.800. En comparación, los individuos del grupo 1 después de la primera dosis mostraron títulos con una mediana de 200 (Figura 1).

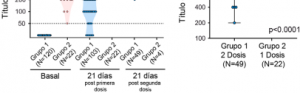
Figura 1. Título de IgG anti-Spike en individuos naive y previamente infectados con SARS-CoV-2 en función del tiempo de administración de la vacuna Sputnik V (grupo 1 y grupo 2, respectivamente). Figura 2. Comparación de los títulos de IgG entre los individuos naive que recibieron dos dosis de la vacuna Sputnik V y los individuos previamente infectados y vacunados con una sola dosis, (p<0,0001, Mann-Whitney test).
Segunda dosis: La respuesta inmune observada 21 días después de la segunda dosis muestra un aumento significativo del título de anticuerpos en todos los voluntarios del grupo 1. La mediana de títulos entre la primera y segunda dosis de este grupo fue de 200 y 1.600, respectivamente (p<0,001). En el grupo 2, por el contrario, no se observaron diferencias significativas cuando se compararon las medianas de los títulos obtenidos después de cada dosis (Figura 1).
Diversos trabajos realizados con las vacunas de Pfizer y Moderna han mostrado recientemente que la respuesta humoral luego de una dosis en personas con exposición previa al virus es de tal magnitud que se sugiere no aplicar una segunda dosis (3-8). Sin embargo no hay estudios hasta el momento con la vacuna Sputnik V que comparen los niveles de respuesta inmune de
individuos vacunados con dos dosis con individuos vacunados con una dosis con exposición previa a SARS-CoV-2.
En el contexto del presente estudio observamos que la mediana de títulos de anticuerpos en personas previamente infectadas que recibieron una sola dosis de vacuna es 8 veces superior al de aquellos voluntarios sin infección previa que recibieron el protocolo completo de vacunación de dos dosis (Figura 2). Estos resultados muestran que la respuesta humoral de memoria de personas previamente expuestas al virus es robusta y significativamente superior a la respuesta observada con dos dosis de vacuna Sputnik V en personas naive (p<0,001). Las medianas de títulos de IgG observadas en el grupo 2 con una dosis y en el grupo 1 con dos dosis, fueron 12.800 y 1.600, respectivamente.
Con el fin de extender la evaluación de la respuesta humoral generada por vacunación con Sputnik V, se realizó la cuantificación de anticuerpos neutralizantes en las muestras obtenidas. Para ello se cuantificaron los anticuerpos capaces de neutralizar el proceso de infección viral en células en cultivo empleando el sistema de virus pseudotipados con la proteína Spike y el virus cepa salvaje.
Los resultados obtenidos indican que los títulos de anticuerpos neutralizantes del grupo 1 muestran medianas de 0, 8 y 30, en el nivel basal, luego de la primera y de la segunda dosis, respectivamente. En el caso de los individuos del grupo 2, previamente infectados, se ve un rápido aumento y de mayor magnitud después de la primera dosis, alcanzando títulos con mediana de 640 y sin observar aumento después de la segunda dosis (Figura 3).
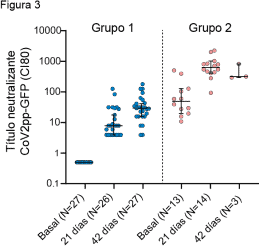
Cabe destacar que si comparamos los títulos de anticuerpos neutralizantes de voluntarios del grupo 1 que recibieron dos dosis con aquellos del grupo 2 que recibieron una dosis, se observan medianas de títulos significativamente diferentes de 30 y 640 (p<0.0001 Mann Whitney), respectivamente, confirmando una mayor respuesta humoral en individuos previamente expuestos al SARS-CoV-2.
Figura 3. Título de anticuerpos neutralizantes en individuos naive y previamente infectados con SARS CoV-2 en función del tiempo de administración de la vacuna Sputnik V. Se muestra la concentración inhibitoria 80 (CI80)
Asimismo se empleó el virus cepa salvaje para evaluar la capacidad de los sueros de los individuos vacunados de neutralizar la infección viral empleando un set de muestras del presente estudio. Los resultados obtenidos indican que las medianas de títulos de anticuerpos neutralizantes en el grupo 1 aumentan de 16 a 64 cuando se compara la respuesta después
de 1 o 2 dosis (aumento de 4 veces; p<0,001). En contraste los datos obtenidos en el grupo 2, con previo contacto con el virus, las medianas de títulos de anticuerpos neutralizantes en el punto basal y 21 días después de la primera dosis son 64 a 1.024, mostrando un aumento de 16 veces (p<0,0001), datos que se correlacionan con la medida de anticuerpos totales contra Spike y anticuerpos neutralizantes empleando el sistema de virus pseudotipados (Figura 4).
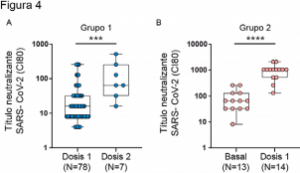
Figura 4. Título de anticuerpos neutralizantes evaluados mediante ensayos con la cepa salvaje SARS-CoV 2 A. Aumento de los anticuerpos neutralizantes en individuos naive entre la 1ra y 2da dosis (p=0,0006, Mann Whitney test). B. Aumento de los anticuerpos neutralizantes en individuos previamente infectados entre la muestra basal y la 1ra dosis (p<0,0001, Mann Whitney test).
Conclusiones: En conjunto los resultados aquí presentados muestran que la vacuna Sputnik V induce una respuesta humoral contra la proteína Spike en el 100% de los voluntarios analizados 21 después de la segunda dosis. Por otro lado, el aumento en el título de anticuerpos IgG totales contra Spike y neutralizantes en individuos con previa exposición al virus que recibieron una dosis de la vacuna fue superior a la observada en individuos naive con las dos dosis. Estos resultados también sugieren que la infección previa genera memoria inmunológica que se evidencia con la primera dosis de Sputnik V y la reactivación de las células de memoria para la producción de niveles incrementados de anticuerpos en comparación con individuos no infectados previamente.
Los datos obtenidos en el presente trabajo sugieren revisar el esquema de vacunación para aquellos individuos que ya han estado expuestos a SARS-CoV-2. La implementación de una sola dosis de vacuna Sputnik V en este grupo no impactaría en la respuesta humoral desarrollada en estos individuos, disminuyendo la incomodidad para este grupo de tener que recibir una dosis adicional y liberando dosis de vacunas para otros usos prioritarios.
Por último, considerando los resultados de Libster y col que demostraron la eficacia en la administración temprana de plasma de convaleciente con altos títulos de anticuerpos (9), en coincidencia con Molly y col (10), se podría evaluar la posibilidad de considerar como donantes a aquellas personas que hayan tenido un diagnóstico de COVID-19 y estén vacunadas con una o dos dosis.
Referencias
- Logunov DY, Dolzhikova I V, Shcheblyakov D V, Tukhvatulin AI, Zubkova O V, Dzharullaeva AS, et al.
Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia. Lancet. 2021;397: 671–681. doi:10.1016/s0140-6736(21)00234-8
- Ojeda DS, Gonzalez Lopez Ledesma MM, Pallarés HM, Costa Navarro GS, Sanchez L, Perazzi B, et al. Emergency response for evaluating SARS-CoV-2 immune status, seroprevalence and convalescent plasma in Argentina. PLOS Pathog. 2021;17: e1009161. doi:10.1371/journal.ppat.1009161
- Krammer F, Srivastava K, Team P, Simon V, Alshammary H, Amoako A, et al. Robust spike antibody responses and increased reactogenicity in seropositive individuals after a 1 single dose of SARS-CoV-2 mRNA vaccine. [cited 25 Feb 2021]. doi:10.1101/2021.01.29.21250653
- Zaytsev P, Hasaneini SJ, Ruina A. Immunogenicity after the First Dose of the BNT162b2 mRNA COVID 19 Vaccine: Real-World Evidence from Greek Healthcare Workers. 2015.
- Samanovic MI, Cornelius AR, Wilson JP, Karmacharya T, Gray-Gaillard SL, Allen JR, et al. Poor antigen-specific responses to the second BNT162b2 mRNA vaccine dose in SARS-CoV-2-experienced individuals. medRxiv Prepr Serv Heal Sci. 2021 [cited 25 Feb 2021]. doi:10.1101/2021.02.07.21251311
- Saadat S, Zahra ;, Tehrani R, Logue J, Newman M, Frieman MB, et al. Single Dose Vaccination in Healthcare Workers Previously Infected with SARS-CoV-2. medRxiv. 2021; 2021.01.30.21250843. doi:10.1101/2021.01.30.21250843
- Levi R, Azzolini E, Pozzi C, Ubaldi L, Lagioia M, Mantovani A, et al. A cautionary note on recall vaccination in ex-COVID-19 subjects. medRxiv. 2021; 4. doi:10.1101/2021.02.01.21250923
- Abu Jabal K, Ben-Amram H, Beiruti K, Batheesh Y, Sussan C, Zarka S, et al. Impact of age, ethnicity, sex and prior infection status on immunogenicity following a single dose of the BNT162b2 mRNA COVID-19 vaccine: real-world evidence from healthcare workers, Israel, December 2020 to January 2021. Eurosurveillance. 2021;26: 1–5. doi:10.2807/1560-7917.es.2021.26.6.2100096
- Libster R, Pérez Marc G, Wappner D, Coviello S, Bianchi A, Braem V, y col ; Fundación INFANT– COVID-19 Group. Early High-Titer Plasma Therapy to Prevent Severe Covid-19 in Older Adults. N Engl J Med. 2021 Feb 18;384(7):610-618. doi: 10.1056/NEJMoa2033700. Epub 2021 Jan 6. PMID: 33406353; PMCID: PMC7793608.
- Molly A. Vickers , Alan Sariol , Judith Leon , Alexandra Ehlers , Aaron V. Locher , Kerry A. Dubay , Laura Collins , Dena Voss , Abby E. Odle , Myrl Holida , Anna E. Merrill , Stanley Perlman , C. Michael Knudson. Exponential increase in neutralizing and spike specific antibodies following vaccination of COVID-19 convalescent plasma donors. medRxiv 2021.02.02.21250836;
doi:https://doi.org/10.1101/2021.02.02.21250836
El trabajo fue realizado por:
Andres Rossi, Anabel Alvarez Juliá, Diego Ojeda, Lautaro Sanchez, Maria Mora Gonzalez Lopez Ledesma, Horacio Pallarés, Guadalupe Costa Navarro, Natali Rasetto, Corina Garcia, Shirley Wenker, Lila Ramis, Magali Bialer, Maria Jose de Leone, Esteban Hermano, Santiago Sosa, Luciana Bianchimano, Maria Soledad Treffinger, Marcelo Yanovsky, Julio Caramelo, Andrea Gamarnik (FIL IIBBA CONICET)
Augusto Varese, Ignacio Mazzitelli, Jorge Geffner (INBIRS- Biobanco)
Guillermo Docena (IIFP, FCE UNLP) Alejandro Aliello, Alejandro Orlowsky (CIC-Medicina UNLP) Marina Pifano, Soledad González, Enio García, Lorena Regairaz, Nicolás Kreplak Min Sal Provincia de Bs As
Hospitales:
HIEAC “San Juan de Dios”: Regina Ercole, Andrea Gatelli, Sofia Di Bella, Agustina Martinez, Martina Ferioli, Francisco Echeverria, Ramiro Agüero, Ana Caproli, Karina Gil
HIGA “Dr. Rodolfo Rossi”: Cecilia Etchegoyen, Claudia Varela, Ángeles Baridon, Soledad Ocampo, Emanuel Zapata, Melina Cancela y Verónica Forneris
HIGA “San Martín”: Susana Marchetti, Sebastián Gutiérrez, María Maxwell, Rosario Marcó, Cecilia Zolorzano, Micaela Nieva, Claudia Conta
HIGA “Evita”: Alejandra Rima, Silvina Olivera, Isabel Desimone, Alejandra Musto
HIGA “Dr. Pedro Fiorito”: Aime Balanzino, Dariana Pedroza, Katherina Prost, Miriam Pereiro, Eliana Correa, Noelia Portillo, Cynthia Leguizamon, Alicia Quetglas
HIGA “San Roque”: Mariana Artazcoz, Paula Gelpi, Agustina Venturi Grossi, Rosana Toro, Anabella Masci, Sofía Padín
HAC “El Cruce- Néstor Kirchner”: Martín Zubieta, Mabel Skrypnik, Blanca Guevara, Virginia Aniasi, Alan Estigarribia